Профилактика лучевых реакций у пациентов со злокачественными опухолями головы и шеи

Авторы: Л. Б. Пархоменко, Н. И. Крутилина, О. В. Красько
Лучевая терапия как в самостоятельном виде, так и в комбинации с химиотерапией и операцией применяется практически у всех пациентов со злокачественными новообразованиями органов головы и шеи и сопровождается развитием ранних лучевых реакций нормальных тканей. Наиболее частым и значимым ранним осложнением консервативного лечения рака органов головы и шеи является мукозит – повреждение слизистой оболочки полости рта и глотки.
По данным различных литературных источников, мукозиты III–IV степени встречаются в 34–100%. Тяжесть мукозита связана с суточной дозой лучевой терапии, суммарной кумулятивной дозой, объемом облученных тканей, использованием сопутствующих химиотерапевтических препаратов, а также зависит от возраста и пола пациента, состояния гигиены его полости рта.
Клинически мукозит проявляется гиперемией и отеком слизистой оболочки, в дальнейшем появляются изъязвления и фибринозный налет, усиливается боль и сухость во рту. Все это приводит к нарушению жевания, глотания и артикуляции, отказу от приема пищи, потере веса. Пациент становится раздражительным, появляются проблемы в семейной и социальной сфере, снижается качество его жизни. Коррекция лучевых повреждений может потребовать зондового питания, интенсивной поддерживающей терапии, а также незапланированных перерывов в лечении, что удлиняет сроки лечения таких пациентов и снижает эффективность специальной терапии.
Для решения проблем, вызванных лучевым повреждением нормальных тканей, применяют как локальные воздействия, так и системные медикаментозные средства с использованием противовоспалительных, антимикробных и обезболивающих препаратов, антиоксидантов и радиопротекторов, колониестимулирующих факторов роста и кератиноцитов.
Нефармакологические методы включают местное охлаждение тканей полости рта. Большое внимание уделяется гигиеническому уходу за полостью рта пациента, лечению кариозных зубов, наличию зубных протезов, соответствующей щадящей диете.
Одним из путей снижения выраженности лучевых реакций является создание гипоксии с целью преимущественной защиты нормальных тканей посредством перитуморального внутритканевого введения вазоактивных веществ или вдыхания обедненных кислородом газовых смесей (например, смеси, содержащей 10% кислорода) или наложением жгута выше зоны облучения.
К физическим методам профилактики и лечения ранних посттерапевтических реакций нормальных тканей относится воздействие низкоэнергетическим лазерным излучением. Перспективным направлением является разработка метода с одновременным использованием лазерного излучения и магнитных полей. Низкоинтенсивная лазерная терапия нормализует окислительно-восстановительные и биосинтетические процессы тканей, восстанавливая микроциркуляцию крови и лимфы, улучшая репаративные процессы в тканях, вызывая обезболивающее, противовоспалительное, сосудорасширяющее, иммунорегулирующее и антигиперкоагуляционное действие.
Магнитотерапия позволяет улучшить общее состояние, повысить устойчивость к различным неблагоприятным факторам, в том числе к радиационному облучению, и расширить компенсаторные возможности организма. Кроме того, магнитотерапия оказывает обезболивающее, противоотечное, седативное, гипотензивное действие, интенсифицирует обменные процессы, улучшает микроциркуляцию, трофику и регенерацию тканей. При одновременном применении этих двух модальностей, происходит более глубокое проникающее воздействие их в окружающие ткани.
До настоящего времени не разработано общепринятых протоколов профилактики и лечения ранних посттерапевтических реакций нормальных тканей. Применяются попытки по обзору опубликованных статей с результатами клинических испытаний определить наиболее эффективные методы, снижающие частоту тяжелых лучевых повреждений. Так, периодически обновляются руководства по лечению мукозитов, разработанные исследовательской группой по мукозитам MASCC/ISOO (Многонациональная ассоциация поддерживающей терапии при раке/Международное общество оральной онкологии).
На современном этапе MASCC/ISOO рекомендует или предлагает (в зависимости от уровня подтверждающих данных) мероприятия по профилактике или лечению острых мукозитов в конкретных ситуациях. Уход за полостью рта является ключевым фактором в профилактике и снижении выраженности мукозита. Другие профилактические меры включают криотерапию, фактор роста кератиноцитов, бензидаминовую жидкость для полоскания рта и цинк. В этот список входит и низкоуровневая лазеротерапия.
С учетом этих рекомендаций и с целью повышения эффективности ранней медицинской реабилитации пациентов со злокачественными новообразованиями органов головы и шеи при проведении лучевой/химиолучевой терапии, нами разработан комплексный подход с использованием медикаментозных, химических и физических агентов для снижения радиопоражаемости окружающих нормальных тканей.
Материал и методы
Дизайн исследования. В 2010–2012 гг. на базе ГУ «РНПЦ онкологии и медицинской радиологии им. Н.Н. Александрова» было проведено рандомизированное проспективное клиническое исследование по изучению применения магнитолазерной и гипоксической терапии для профилактики развития выраженных лучевых реакций у пациентов со злокачественными опухолями органов головы и шеи.
Критерии включения в исследование: гистологическое подтверждение диагноза плоскоклеточного рака слизистой оболочки полости рта, языка, глотки и гортани II, III или IVА,В стадий; показатель функционального состояния по шкале Карновского более 50% (0-1-2 баллов по шкале ECOG); отсутствие сопутствующей патологии в стадии декомпенсации, а также отсутствие в анамнезе лучевой терапии области головы и шеи и/или курсов химиотерапии по поводу другого злокачественного новообразования. Все пациенты дали письменное информированное согласие.
Пациенты. В исследование включены 160 пациентов. До начала рандомизации у 60 пациентов, не включенных в заключительный анализ, проводилась отработка методик профилактики и лечения ранних лучевых реакций с использованием магнитолазерной и гипоксической терапии в различных режимах. Формирование групп с целью сравнительного изучения эффективности ранней медицинской реабилитации, включающей стандартные подходы и новые методики профилактики и лечения ранних лучевых реакций, было начато после установления отсутствия каких-либо побочных эффектов применения магнитолазеротерапии и фармакологически индуцированной локальной гипоксии во время курса лучевой терапии.
В рандомизированное проспективное исследовании было включено 100 пациентов в возрасте 32–76 лет. Один пациент после подписания информированного согласия и прохождения рандомизации отказался от дальнейшего участия в клиническом исследовании. Один пациент выбыл из протокола исследования из-за обострения сопутствующей сердечно-сосудистой патологии после первого введения цисплатина в начале курса лучевой терапии.
Оставшиеся 98 пациентов были распределены в четыре группы (одна контрольная и три основных) на основании использования различных методик профилактики и лечения ранних лучевых реакций нормальных тканей в рамках системы ранней медицинской реабилитации.
После рандомизации в группу «Контроль» вошли 32 пациента. Из них у 6 пациентов установлен диагноз рака дна полости рта/тела языка, у 14 пациентов – рака ротоглотки, и по 6 пациентов имели диагноз рака гортаноглотки и гортани.
В группу «Магнитолазер» вошли 20 пациентов. Диагноз рака слизистой полости рта или тела языка имели 5 пациентов, диагноз рака ротоглотки – 6 пациентов, диагноз рака гортаноглотки – 2 пациента. У 7 пациентов установлен диагноз рака гортани.
В группу «Гипоксия» вошли 25 пациентов. Диагноз рака слизистой полости рта или тела языка был установлен в 6 случаях, ротоглотки – в 13, а гортаноглотки – в 5 случаях. В одном наблюдении был выявлен диагноз рака гортани.
В группу «Комплекс» вошел 21 пациент. Локализацию рака в полости рта и подвижной части языка имели 2 пациента. Диагноз рака ротоглотки зафиксирован у 13 пациентов, гортаноглотки – у 2 пациентов. У 4 пациентов установлен диагноз рака гортани.
Всем пациентам проводилась дистанционная конформная лучевая терапия в классическом режиме фракционирования дозы излучения РОД 2 Гр, 1 раз в день, 5 раз в неделю, 35 фракций, до суммарной очаговой дозы 66–70 Гр на первичный очаг и СОД 50–70 Гр на регионарные лимфатические узлы шеи.
Химиолучевую терапию получало 70% пациентов, включенных в исследование, с внутривенной инфузией цисплатина 100 мг/м2 в 1-й, 22-й и 43-й дни облучения.
Методики профилактики и лечения ранних лучевых реакций. В первой группе «Контроль» в течение всего курса лучевой терапии осуществлялась санация ротовой полости антисептическими растворами 8–10 раз в день (отвар шалфея, ромашки и др.). При развитии умеренной болезненности в полости рта и глотке, обусловленной лучевыми реакциями, осуществляли аппликации препаратов, обладающих местным обезболивающим действием: 1–2% раствор лидокаина, анастезина, новокаина.
Во второй группе «Магнитолазер» с 3-го дня облучения назначалась магнитолазерная терапия (аппарат “РИКТА”). Воздействие осуществляли на облучаемые ткани (слизистая оболочка полости рта и ротоглотки, кожные покровы) через 60 мин. после сеанса лучевой терапии сканирующим методом с зазором между излучателем и облучаемыми тканями 0,5–1,0 см. Длительность процедуры: 5–7 мин. Курс лечения: 15 процедур через день. Частота воздействия составляет 1000 Гц (импульсная мощность лазера 8 Вт).
В третьей группе «Гипоксия» проводилась местная гипоксическая терапия путем локального применения альфа-адреноблокатора. За 10 мин до проведения сеанса лучевой терапии осуществляли орошение визуально неизмененной слизистой оболочки полости рта спреем ксилометазолина гидрохлорида 0,1%. (максимальная доза до 4-х впрыскиваний).
В четвертой группе «Комплекс» осуществлялась комплексная терапия, включающая гипокситерапию до сеанса облучения и магнитолазерную терапию после сеанса лучевой терапии по приведенным выше методикам.
Конечные точки исследования. В качестве конечных точек использовались показатели острой токсичности слизистой оболочки и кожи, вошедшие в объем облучения. Выраженность ранних лучевых реакций нормальных тканей оценивалась по шкале EORTC/RTOG: 0 степень – без изменений, 1–4 степени – различная по возрастанию выраженность лучевых реакций, 5 степень – смерть от лучевых осложнений.
Фиксировалась максимальная степень лучевых реакций слизистых оболочек полости рта и глотки, а также кожных покровов в области облучения после окончания курса лучевой терапии.
Вторичные конечные точки включали безопасность лечения, изменение функций глотания, подвижности нижней челюсти, массы тела и выраженности боли в процессе лучевого лечения. Изучение этих данных проводилось перед началом лучевой терапии и сразу после завершения курса лучевого лечения.
Функция глотания исследовалась по 4-х балльной шкале: 0 баллов – нет затруднения при глотании; 1 балл – затруднения при проглатывании твердой пищи, при этом, человеку приходится постоянно запивать съеденные кусочки пищи; 2 балла – затруднение при проглатывании полужидкой пищи (каши, пюре); 3 балла – затруднение при проглатывании жидкости (вода, чай); 4 балла – непроходимость любой пищи.
Подвижность нижней челюсти была оценена по 3-х балльной шкале: 0 баллов – рот открывается свободно, без ограничений; 1 балл – открывание рта слабо ограничено, расстояние между центральными резцами верхней и нижней челюсти 3–4 см; 2 балла – ограничение открывания рта в пределах 1–1,5 см; 3 балла – рот открывается не более чем на 1 см.
Изменение интенсивности боли во время курса лучевой терапии изучено по десятибалльной визуально-аналоговой шкале (ВАШ).
Статические методы
Сравнения реабилитационных показателей в группах до и после ЛТ проводились по критерию предельной однородности при повторяющихся измерениях.
Сравнения групп по реабилитационным показателям проводились по критерию хи-квадрат, в случае нарушения предположений, лежащих в основе критерия хи-квадрат, использовался критерий Фишера. Для последующих попарных сравнений применялась поправка Хольма на множественные сравнения для предотвращения ложноположительных результатов в рамках заданной ошибки первого рода. Результаты считались статистически значимыми при p < 0,05.
Результаты и обсуждение
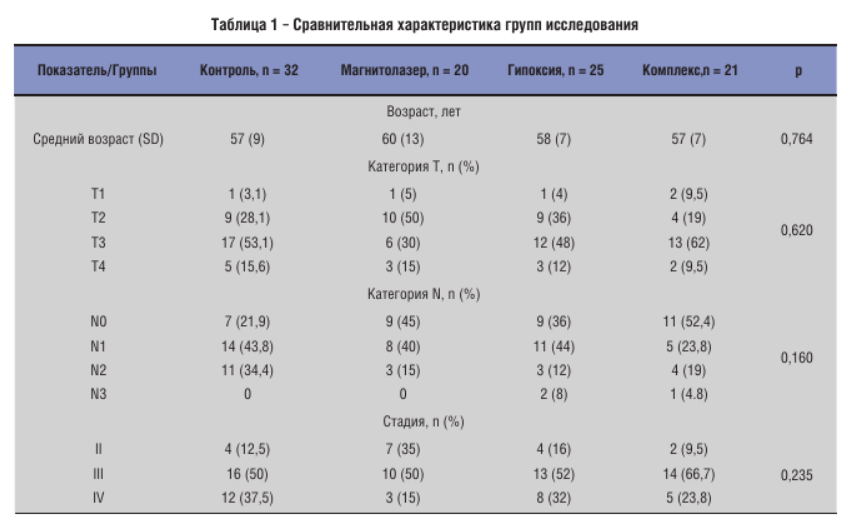
При сравнении групп исследования по возрасту и степени распространенности опухолевого процесса не было выявлено статистически значимых различий. Характеристика групп исследования представлена в таблице 1:
Безопасность. Во всех группах исследования не было ни одного случая смерти от лучевых осложнений (V степень). Все пациенты, которым проводились разработанные реабилитационные мероприятия, завершили запланированный курс лучевой терапии без продолжительных перерывов в специальном лечении. Серьезных побочных реакций общего или местного характера ни в одной из групп пациентов не выявлено.
Ранние лучевые реакции. Установлено, что 87,5% пациентов контрольной группы, которым в системе ранней медицинской реабилитации применялись традиционные медикаментозные средства, имела 2-ю и 3-ю степень выраженности лучевых реакций слизистой оболочки.
В отличие от остальных групп, в контрольной группе не наблюдалось лучевых реакций 0-й и 1-й степени, однако встречались серьезные осложнения 4-й степени (12,5%).
По сравнению с контролем в основных группах определяется статистически значимые различия в частоте и выраженности ранних лучевых реакций слизистых оболочек (р < 0,001 для группы с магнитолазерной и комплексной терапией; р < 0,002 для группы с гипоксической терапией).
Сведения о развитии ранних лучевых реакций слизистых оболочек полости рта по окончании курса лучевой терапии у включенных в исследование пациентов представлены на рисунке 1:
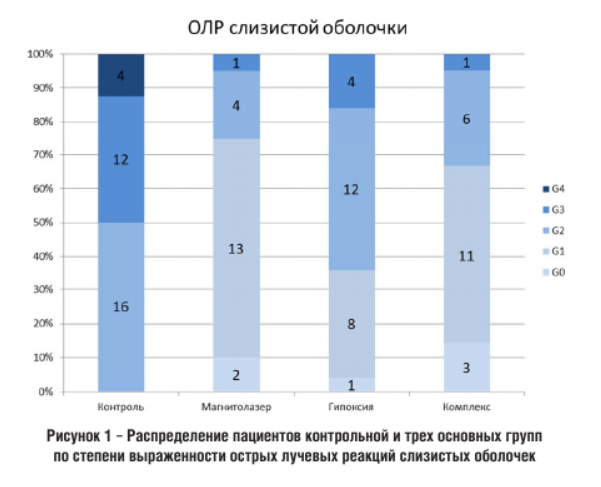
При сравнении активного воздействия между собой с определением p-value (c поправкой на множественные сравнения) установлена корреляция между количеством/степенью ранних лучевых реакций слизистых оболочек и методом профилактики в основных группах. В итоге по результатам изучения острых лучевых реакций слизистых оболочек, между основными группами исследования значимых различий не наблюдалось, хотя наметилась тенденция к снижению частоты и тяжести мукозитов при использовании магнитолазерной терапии.
Результаты комплексного воздействия незначительно отличались от ее результатов (р = 0,860). Гипоксическая терапия приводила к более частым и выраженным реакциям по сравнению как с магнитолазерной терапией (р = 0,203), так и с комплексной терапией (р = 0,423) без статистически значимых различий.
Результаты анализа ранних лучевых реакций кожи по окончании курса лучевой терапии у включенных в исследование пациентов представлены на рисунке 2:
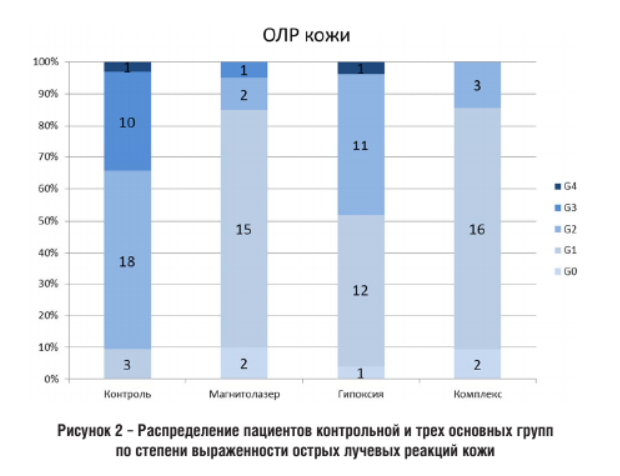
У пациентов контрольной группы не была выявлена 0 степень кожных реакций. В единичных случаях отсутствие кожных изменений наблюдалось во всех трех основных группах исследования. Преобладающее большинство пациентов групп «Магнитолазер» и «Комплекс» имели 1-ю степень лучевых реакций кожи – соответственно 75% и 76,2%. А в группе «Гипоксия» практически одинаково часто встречались реакции 1-й (48%) и 2-й (44%) степеней.
В контрольной группе чаще наблюдались реакции 2-й (56,2%) и 3-й (31,2%) степеней выраженности. По срав- нению с контролем во всех трех основных группах выявлены статистически значимые различия (р < 0,001).
При сравнении групп между собой, лучшие показатели наблюдались в группах «Магнитолазер» и «Комплекс» без каких-либо существенных различий между ними (> 0,99).
В отличие от этих групп, гипоксическая терапия показала тенденцию меньшей эффективности в сравнении с магнитолазерным (р = 0,082) и комплексным (р = 0,107) лечением.
При изучении гематологической токсичности по показателям периферической крови (лейкоциты), статистически значимых различий между всеми группами исследования выявлено не было (> 0.99), хотя наблюдается тенденция к меньшему развитию гематологических изменений в группе «Магнитолазер» – у 85% пациентов этой группы количество лейкоцитов в периферической крови не изменилось, что наглядно представлено на рис. 3:
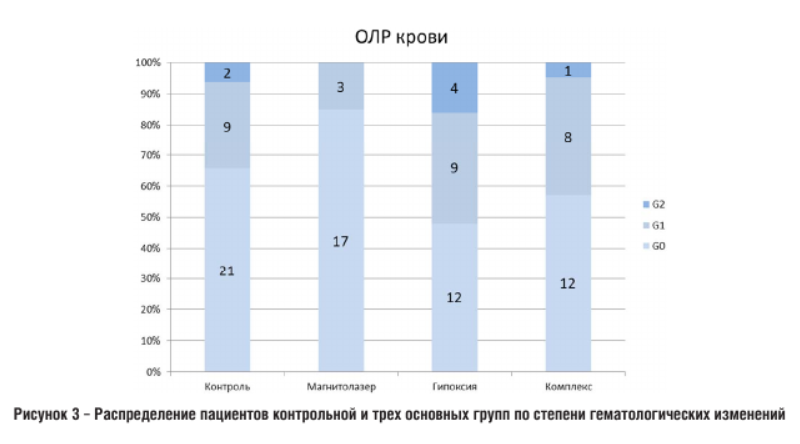
Вероятнее всего, это связано с тем, что в настоящем исследовании при общем количестве случаев применения химиолучевой терапии равном 70% в группе «Магнитолазер» воздействие двух лечебных модальностей встречалось в 60%, в остальных группах – в 75%. А развитие гематологической токсичности связано в первую очередь с системным воздействием химиотерапевтического препарата. Теоретически, а в нашем исследовании и практически, применение лучевой терапии с химиотерапией приводит к более выраженным изменениям показателей крови, чем использование одной только лучевой терапии. Хотя в целом статистически значимой разницы между группами получено не было.
Анализ функции глотания. При изучении глотания перед началом специального лечения группы не различались (p = 0,607). У 65% пациентов группы «Магнитолазер» и у 60% пациентов в остальных группах не было затруднений при глотании. После завершения курса лучевой терапии все три основные группы отличались от группы контроля со статистически значимой разницей (р < 0,001). Однако между группами с применением разрабатываемых мероприятий по снижению лучевых реакций значимых различий не наблюдалось (р > 0,99).
Что касается изменения глотания внутри каждой группы, то более выраженные затруднения в глотании после окончания курса лучевой терапии испытывали пациенты контрольной группы (<0,001). В группах с применением различных разрабатываемых схем ранней медицинской реабилитации серьезных изменений функции глотания с трудностями при проглатывании жидкой пищи не наблюдалось, хотя в каждой из этих групп после завершения курса лучевой терапии выявлено статистически значимое (р <0 ,05) нарушение глотания по сравнению с началом лечения (рис. 4):
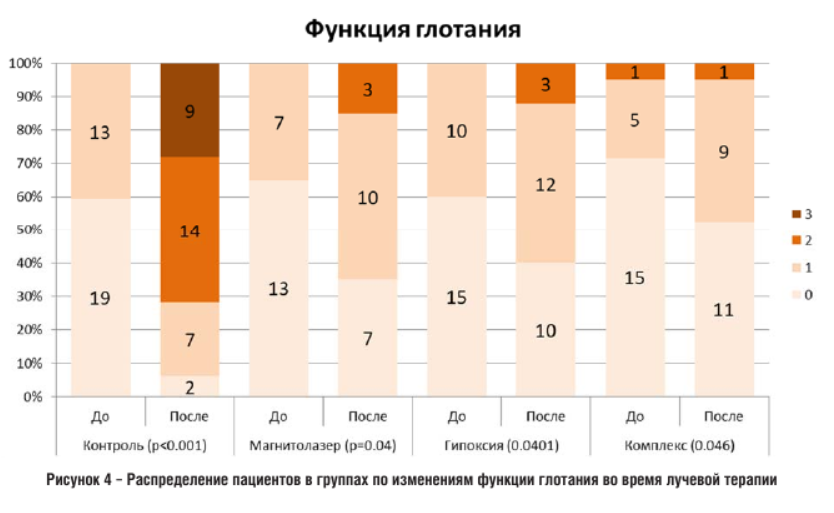
Анализ подвижности нижней челюсти. Перед началом лечения группы были однородны по степени нарушения подвижности нижней челюсти (p = 0,302). После завершения курса лучевой терапии все три основные группы статистически значимо не отличались от группы контроля: «Магнитолазер» (р = 0,247), «Гипоксия» (р = 0,460), «Комплекс» (р = 0,440), а также между собой (> 0,99). При изучении изменений функции нижней челюсти внутри каждой группы, статистически значимое снижение ее подвижности после окончания курса лучевого лечения было получено только в группе «Контроль» (р = 0,002). В трех основных группах подвижность нижней челюсти была сохранена практически у всех пациентов на первоначальном уровне (рис. 5):
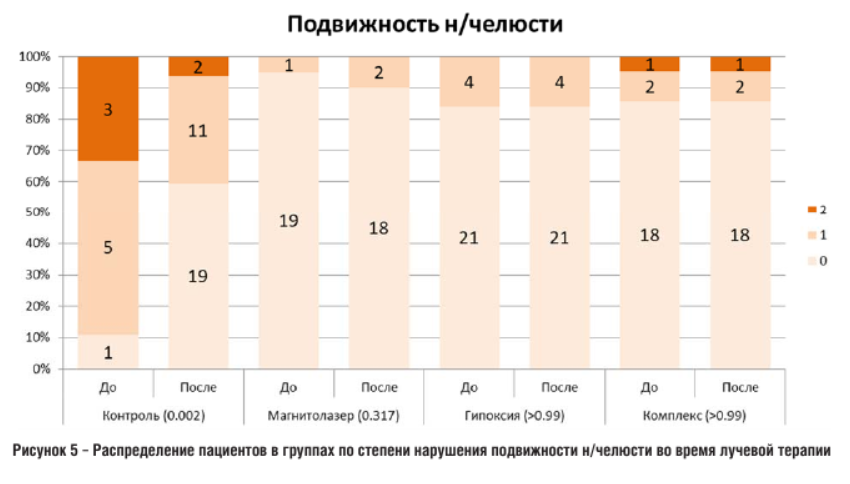
Анализ изменения массы тела. При изучении изменения массы тела в процессе лучевой терапии было выявлено, что пациенты контрольной группы к концу лучевой терапии чаще теряли вес около 10% от исходного, в то время у пациентов трех основных групп более чем в половине случаев потеря массы тела на момент завершения лучевой терапии составляла менее 5%. Изменение массы тела пациентов всех групп исследования в процессе лучевой терапии представлена в таблице 2:
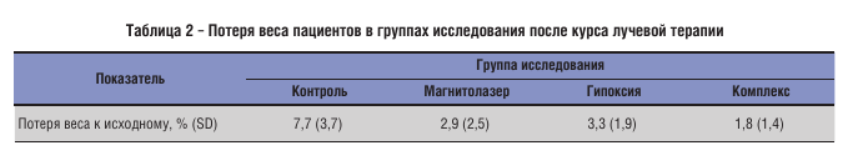
Как видно из таблицы, по такому признаку как изменение массы тела все три основные группы статистически значимо отличаются от контрольной группы (р < 0.001). При сравнении основных групп между собой таких больших различий в потере веса мы не выявили. А использование магнитолазера и гипоксии по отдельности привело к практически одинаковым результатам (р = 0,961).
Анализ интенсивности боли. Проведен анализ изменения интенсивности боли во время курса лучевой терапии. В таблице 3 представлено количество пациентов в каждой группе с исходной оценкой болевого синдрома перед лечением и после проведенной лучевой терапии.
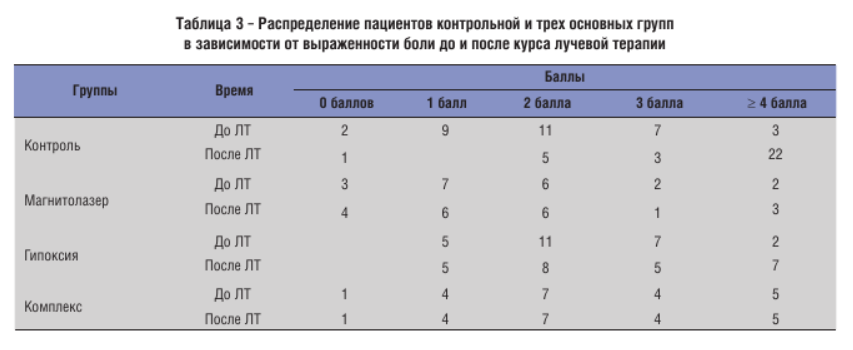
До лучевой терапии по выраженности боли все группы были однородны (р = 0,613). После лечения основные группы статистически значимо отличались от контроля, но не между собой. Лучшие результаты были получены в группе с применением магнитолазерной терапии (р < 0,001).
Гипоксическая терапия в меньшей степени справлялась с нарастанием болевого синдрома во время курса радиотерапии, чем магитолазер, однако статистически значимой разницы между этими группами не получено (р = 0,287). При изучении изменений болевого синдрома внутри каждой группы, значительное нарастание боли к концу курса лучевой терапии наблюдалось только в группах «Контроль» (р < 0,001) и «Гипоксия» (р = 0,018).
Перерывы в специальном лечении. Все пациенты завершили запланированный курс лучевой терапии. В основных группах наблюдались непродолжительные перерывы в специальном лечении, в отличие от контрольной группы, где перерывы для лечения лучевых реакций были более продолжительными и частыми.
В группе с применением магнитолазерной терапии у 1 пациента (5%) был сделан трехдневный перерыв в специальном лечении. В группе с применением гипоксии у 1 (4%) пациента был сделан четырехдневный перерыв в специальном лечении. В группе с применением комплексной терапии у 2 пациентов (9%) были сделаны 3- и 4-дневный перерывы в специальном лечении. В контрольной группе пациентов в 10 случаях (31%) были сделаны перерывы в специальном лечении от 3 до 11 дней (среднее количество дней = 5,9).
Выводы
Таким образом, применение разработанных методик профилактики и лечения ранних лучевых реакций нормальных тканей с использованием магнитолазерной и гипоксической терапии самостоятельно или одновременно статистически значимо снижает частоту и выраженность лучевых изменений нормальных тканей и органов во время курса лучевого лечения.При сравнении основных групп между собой по ранним лучевым реакциям нормальных тканей статистически значимой разницы не обнаружено. Однако, менее выраженные ранние лучевые реакции слизистых оболочек и кожи наблюдались при применении магнитолазерной терапии как в самостоятельном виде, так и в комплексе с гипоксической терапией.
Одинаково эффективными для сохранения глотания и подвижности нижнечелюстного сустава оказались все три разрабатываемых варианта медицинской реабилитации. По изменениям функции этих органов существенная разница наблюдалась только по отношению к контрольной группе всех трех основных групп.
По изменению массы тела и интенсивности боли в конце курса лучевой терапии все три основные группы статистически значимо отличались от контрольной группы, но не между собой. Тем не менее комплексное применение магнитолазера и гипоксии привело к меньшей потери веса по отношению к их использованию в самостоятельном виде; нарастание боли к концу курса лучше всего предотвращала магнитолазерная терапия.
Список литературы:
- Максимов С.А., Мардынский Ю.С., Медведев B.C. и др. Мегавольтная лучевая терапия местнораспространенного рака ротоглотки // Рос. Онкол. Журн. – 2004 – № 2 – С. 18–22.
- Scully C., Epstein J., Sonis S. Oral mucositis: a chall enging complication of radiotherapy, chemotherapy and radiochemotherapy: part 1, pathogenesis and prophylaxis of mucositis // Head & Neck. – 2003 – Vol. 25 – P. 1057–1070.
- Epstein J.B., Silverman S.Jr., Paggiarino D.A. et al. Benzydamine HCI for prophylaxis of radiation-induced oral mucositis: results from a multicenter, randomized, double-blind, placebo-controlled trial // Cancer. – 2001 – Vol. 92 – P. 875–885.
- Epstein J.B., Elad S., Eliav E. et al. Orofacial pain in cancer: part II–clinical perspectives and management // J. Dent. Res. – 2007 – Vol. 86, №6. – Р. 506–518.
- Okuno S., Foote R.L., Olmscheid M.A. et al. Evaluation of an oral capsaicin lozenge for preventing radiation-induced mucositis // J. Cancer Integr. Med. – 2004 – Vol. 2 – Р. 179–183.
- Dahiya M.C., Redding S.W., Dahiya R.S. et al. Oropharyngeal candidiasis caused by non-albicans yeast in patients receiving external beam radiotherapy for head-and-neck cancer // Int. J. Radiat. Oncol. Biol. Phys. – 2003 – Vol. 57 – Р. 79–83.
- Duncan G.G., Epstein J.B., Tu D. et al. Quality of life, mucositis, and xerostomia from radiotherapy for head and neck cancers: a report from the NCIC CTG HN2 randomized trial of an antimicrobial lozenge to prevent mucositis // Head& Neck. – 2005 Vol. 27 – P. 421–428.
- Ferreira P.R., Fleck J.F., Diehl A. et al. Protective effect of alpha-tocopherol in head and neck cancer radiation-induced mucositis: a double-blind randomized trial // Head & Neck. – 2004 – Vol. 26 – P. 313–321.
- Ertekin M.V., Koc M., Karslioglu I. et al. Zinc sulfate in the prevention of radiation-induced oropharyngeal mucositis: a prospective, placebo-controlled, randomized study // Int. J. Radiat. Oncol. Biol. Phys. – 2004 – Vol. 58 – Р.167–174.
- Cerchietti L.C., Navigante A.H., Lutteral M.A. et al. Double-blinded, placebo-controlled trial on intravenous L-alanyl-L-glutamine in the incidence of oral mucositis following chemoradiotherapy in patients with head-and-neck cancer // Int. J. Radiat. Oncol. Biol. Phys. – 2006 – Vol. 65 – Р. 1330–1337.
- Suntharalingam M., Jaboin J., Taylor R. The evaluation of amifostine for mucosal protection in patients with advanced loco-regional squamous cell carcinomas of the head and neck (SCCHN) treated with concurrent weekly carboplatin, paclitaxel, and daily radiotherapy (RT) // Semin. Oncol. – 2004 – Vol. 31, № 18 – P. 2–7.
- Bultzingslowen I., Brennan M.T., Spijkervet F.K. et al. Growth factors and cytokines in the prevention and treatment of oral and gastrointestinal mucositis // Support Care Cancer. – 2006 – Vol. 14, № 6 Р. 519–527.
- Peterson D.E., Ohrn K., Bowen J. et al. Systematic review of oral cryotherapy for management of oral mucositis caused by cancer therapy // Support Care Cancer. – 2013 – Vol. 21 – Р. 327–332.
- Lalla R.V., Sonis S.T., Peterson D.E. Management of Oral Mucositis in Patients with Cancer // Dent. Clin. North Am. – 2008 – Vol. 52, №1. – Р. 61–77.
- Sonis S.T., Hashemi S., Epstein J.B. et al. Could the biological robustness of low level laser therapy (photobiomodulation) impact its use in the management of mucositis in head and neck cancer patients // Oral Oncol. – 2016 – Vol. 54 – Р. 7–14.
- Lalla R.V., Ashbury F.D. The MASCC/ISOO Mucositis Guidelines: dissemination and clinical impact // Support Care Cancer. – 2013 – Vol. 21 – Р. 3161–3163.
- Shankar A., Roy S., Bhandari M. et al. Current Trends in Management of Oral Mucositis in Cancer Treatment // Asian. Pac. J. Cancer Prev. – 2017 – Vol. 18, № 8 – Р. 2019–2026.
Статья для пациентов с диагностированной доктором болезнью. Не заменяет приём врача и не может использоваться для самодиагностики.
по применению аппарата РИКТА